快序荐文
(1) 本研究提出了一种新颖的中和抗体开发思路,借助特定人群对病原的免疫力,从血液中筛选出天然有效的人源中和抗体,用于危重症病人的治疗。
(2) 这类从人体血液中发现的天然抗体序列,经过了血液和免疫系统筛选,具有良好的可开发性。这种抗体发现范式也可推广应用在其他感染性疾病的治疗中。
(3) 除了文中提到的抗体发现路径外,Rapid Novor 快序生物掌握全球唯一的血清多抗测序技术,可以对人血清多克隆抗体蛋白直接测序,发现由血液和免疫系统筛选出的优质天然抗体。

简介
在医院的重症监护室里,一种肉眼看不见的敌人正在悄然肆虐。它就是铜绿假单胞菌(PA),一种能在呼吸机管道、输液针头甚至皮肤表面潜伏的"超级细菌"。更可怕的是,它对大多数抗生素都"刀枪不入",每年在全球范围内夺走无数生命。
然而,最新发表在《eLife》杂志上的一项研究,为这场无声的战争带来了曙光。科学家们从囊性纤维化(CF)患者的血液中提取特殊的免疫细胞,成功制造出能精准摧毁PA的"生物导弹"——单克隆抗体。这种源自人体的天然武器,或许能终结PA感染无药可治的困境。
一、CF患者体内积累了大量PA特异性B细胞
PA的耐药性早已成为医学界的噩梦。这种革兰氏阴性菌拥有一套复杂的防御系统:厚厚的细胞壁能阻挡药物进入,高效的外排泵可将抗生素"扫地出门",甚至能在体内形成生物膜抱团抵抗攻击。据统计,PA引起的医院获得性感染死亡率高达30%~50%,而多重耐药菌株的出现更让治疗雪上加霜。
传统抗生素的研发速度远远赶不上细菌变异的步伐,科学家们将目光转向了人体自身的免疫系统。早在2002年,研究人员就发现,针对PA毒力因子PcrV的抗体能在动物模型中发挥保护作用。PcrV是PAIII型分泌系统的"矛头"蛋白,负责将毒素注入宿主细胞,堪称细菌的 "致命武器"。
但早期临床试验却遭遇滑铁卢:这些抗体大多源自小鼠,进入人体后会被免疫系统识别为 "外来者",不仅疗效大打折扣,还可能引发严重的过敏反应。因此需要开发真正源自人体的抗体,而囊性纤维化患者因经常接触PA,体内积累了丰富的PcrV特异性B细胞,成为了天然中和抗体的重要来源。
CF 患者由于呼吸道黏液黏稠,极易遭受PA的反复感染。令人惊讶的是,他们的适应性免疫功能并未受损,反而在长期与PA的"战斗"中,练就了一套高效的抗体生产系统。研究团队发现,CF患者血液中PcrV特异性 B 细胞的数量,是健康人的数倍之多。这些"经验丰富"的免疫细胞,正是制造强效抗体的关键。
二、从人血液中获得天然抗体序列
为了提取这些珍贵的免疫细胞,研究人员设计了一种特殊的"分子钓钩"——PcrV四聚体荧光探针。这种探针能像磁铁一样,精准捕获血液中所有能识别PcrV的B细胞。通过流式细胞术,科学家们从14名CF患者的外周血中,成功分选出PcrV特异性B细胞。

接下来,研究团队对单个B细胞进行测序,解析出编码抗体的基因序列。令人惊喜的是,这些基因展现出丰富的多样性:有的保留着"原始版本"的germline序列,有的则经过了体细胞高频突变的"升级改造"。其中,一名慢性感染PA的CF患者体内的B细胞,成为了最耀眼的"明星"。

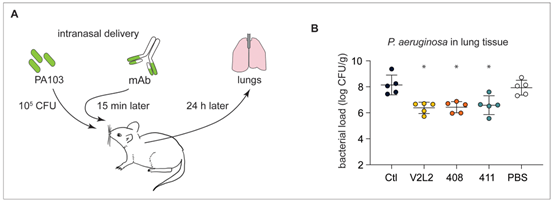
研究人员将这些基因导入293T细胞表达抗体,经过筛选,他们获得了20种不同的单克隆抗体(mAbs),其中7种展现出超高亲和力。更令人兴奋的是,当这些抗体被注入感染PA的小鼠体内后,肺部的细菌负荷竟降低了100倍,效果与经过复杂工程改造的阳性对照抗体V2L2MD不相上下。
三、人源抗体的三大优势:高效、安全、精准
与传统的小鼠源抗体相比,这种人源抗体具有三大核心优势:
高效性:传统方法需要免疫数百只小鼠,筛选数千个杂交瘤细胞才能获得有效抗体;而该研究仅通过12个B细胞序列,就成功获得了具有保护作用的抗体,效率提升数十倍。
安全性:完全人源化的抗体避免了免疫排斥反应,大大降低了过敏风险。在小鼠模型中,这些抗体展现出良好的耐受性,为临床转化奠定了基础。
精准性:这些抗体经过人体免疫系统的"自然筛选",能精准识别PA的关键毒力因子PcrV,避免了对人体正常细胞的误伤。更重要的是,研究团队发现,即使是未经体细胞高频突变的抗体,也能在体内发挥强效保护作用,这为快速应对突发感染提供了可能。
四、未来展望:重塑感染性疾病治疗格局
这项研究的意义远不止于对抗PA。它开创了一种全新的抗体发现模式:从感染患者体内直接获取抗原特异性B细胞,通过单细胞测序和基因工程技术,快速生成人源化单克隆抗体。这种方法可广泛应用于其他耐药菌感染,如鲍曼不动杆菌、金黄色葡萄球菌等。
更令人期待的是,随着抗体开发技术的进一步突破,未来或许能实现"个性化抗体治疗":从患者自身血液中提取B细胞,量身定制专属的抗体药物。这将彻底改变感染性疾病的治疗格局,为免疫力低下人群、重症感染患者带来新的希望。
参考资料
[1] Hale M, Takehara KK, Thouvenel CD, et al. Monoclonal antibodies derived from B cells in subjects with cystic fibrosis reduce Pseudomonas aeruginosa burden in mice. Elife. 2025;13:RP98851. Published 2025 Apr 24. doi:10.7554/eLife.98851