
血清学诊断主要是检测人体针对病毒、细菌或寄生虫疾病所产生的特异性免疫球蛋白,这对于检测既往感染情况、评估免疫状态以及提供预后信息意义重大。传统的血清学检测多采用间接免疫测定法,不过这种方法存在诸多局限,比如只能进行半定量检测、缺乏通用的参考标准、容易出现交叉反应,并且难以对所有同种型和亚型开展多重检测等。倘若能够实现对免疫球蛋白的同种型和亚型进行多重定量分析,采用通用参考标准,同时尽可能减少交叉反应和非特异性结合,那么开
发出诊断特异性更高的检测方法将成为可能,这对于无症状人群的传染病、自身免疫性疾病以及癌症的筛查极为有利。本文详细阐述血清学诊断的主要临床需求、传统和新兴的检测技术,深入剖析质谱技术和免疫亲和蛋白质组学的优势与局限,以及新方法的设计思路[1]。
血清学诊断的临床需求
血清学检测在传染病防控中发挥关键作用,也在癌症早期筛查、自身免疫病精准诊断及不孕症评估中展现出巨大潜力。在传染病领域,其通过抗体检测结合PCR,实现感染阶段判断(如肝炎、梅毒母婴阻断)、输血安全保障(虫媒病毒、细菌和寄生虫)及新发疫情监测(如登革热、COVID-19)。自身免疫病方面,类风湿关节炎、炎性肠病、自身免疫性胃炎、乳糜泻、多发性硬化症、系统性红斑狼疮等疾病依赖抗体的血清学检测。在癌症领域,血清学通过检测肿瘤相关抗原(TAA)的自身抗体,和对不同亚型抗体的分析,可能有助于癌症早期诊断与免疫治疗指导。
传统与新兴免疫测定技术用于血清学诊断
传统免疫测定技术主要依靠抗原-抗体特异性结合来实现病原体检测,但它存在半定量、标准化困难以及交叉反应等问题(图1)。以酶联免疫吸附试验(ELISA)这一成熟方法为例,其检测依赖二抗标记,无法报告抗体的绝对浓度,也很难实现抗体亚型的多重检测。侧向流动免疫分析(LFI)虽然具有便携性,但也存在灵敏度和可重复性较低、半定量以及批次间差异大等缺点。流式荧光技术则能够在单个样本中对数十个指标进行分析,具有稳定性好、可重复性高的优势。一个特殊的案例是多发性骨髓瘤(MM)患者血液内M蛋白的检测,可通过质谱或其他技术进行检测。
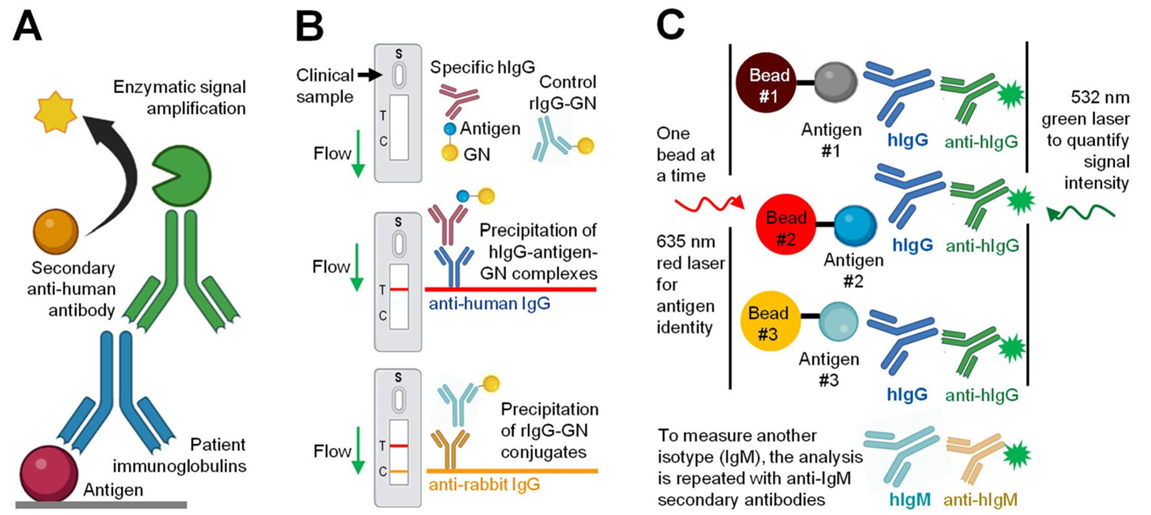
图 1 传统检测技术用于血清学免疫测定
新兴技术,如表面等离子共振(SPR)、生物层干涉技术(BLI)、电化学生物传感器以及蛋白质微阵列等,通过无标记检测、实时动力学分析或者超高通量蛋白互作解析,极大地提升了检测精度和效率(图2)。例如,SPR和BLI能够直接对抗体亲和力进行定量,可以实时监测抗原抗体的结合过程。电化学生物传感器可快速检测生物流体中的蛋白质。蛋白质微阵列则能够同时对数万种蛋白抗原进行分析。不过,新兴技术也面临着设备成本高、标准化不足以及临床转化受限等难题。未来,需要整合传统与新兴方法的优势,推动血清学检测朝着绝对定量、多重分析以及自动化方向发展,以满足复杂疾病精准诊断的需求。
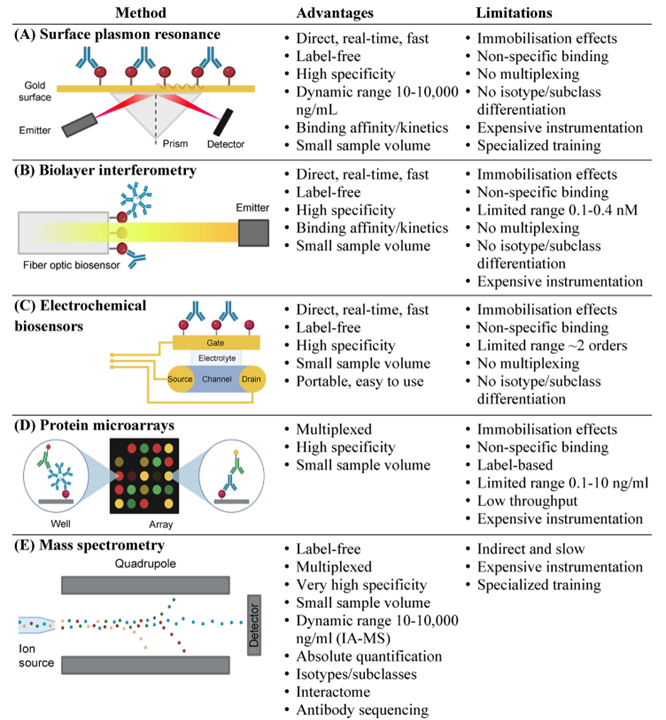
图 2 用于血清学诊断的新兴免疫测定检测技术
免疫亲和质谱技术在血清学诊断中的应用
免疫亲和质谱(IA-MS)技术将免疫亲和富集与质谱(MS)相结合,给血清学检测带来了革命性的突破。其核心原理是利用抗原抗体的特异性结合来捕获目标抗体,经过酶解后通过质谱分析特征肽段,再结合同位素内标实现抗体的绝对定量(图3)。质谱技术凭借多维数据(如质荷比、保留时间等)实现了高特异性检测,克服了传统ELISA半定量和交叉反应的局限,动态范围提升了10倍(以IgG1检测范围为例,可达70-70,000 ng/mL),这使得在检测临床样本时无需多次稀释即可完成检测。但是,该技术同样面临挑战,质谱灵敏度相较于传统免疫测定方法低2-3个数量级,而且抗体亚型的多样性增加了分析的难度。未来,随着自动化流程、快速MALDI-TOF质谱以及标准化同位素肽段的应用,IA-MS有望成为血清学诊断的“金标准”,为传染病、癌症以及自身免疫病的精准诊疗提供有力支持。

图 3 利用免疫亲和靶向蛋白质组学进行血清学诊断
推进免疫亲和蛋白质组学用于抗体测序
单克隆抗体在肿瘤学、自身免疫性疾病以及慢性炎症等领域发挥着重要作用。直接从患者样本中富集病原体特异性抗体并进行测序,有助于快速开发治疗性抗体。然而,由于抗体克隆的多样性,尤其是CDR-H3的高度多样性,使得从头测序面临巨大挑战(图4)。目前已经开发出多种技术尝试抗体从头测序,比如借助单细胞B细胞受体mRNA测序数据库的质谱测序,以及利用神经网络和深度学习解析抗体质谱图等方法,但这些技术都难以真正实现对血清多抗序列的直接从头测序。免疫亲和蛋白质组学有望推动从患者样本中富集高亲和力的抗体进行从头测序。对SARS-CoV-2抗体等的研究发现,一些抗原特异性多克隆抗体库中克隆型数量较少,并且通过抗体测序能够发现一些B细胞RNA测序遗漏的高丰度克隆型。对直接从患者样本中富集的成熟高亲和力和高丰度抗体进行质谱测序,将为治疗性抗体研发、疗法拓展以及精准免疫学研究开辟新的途径。
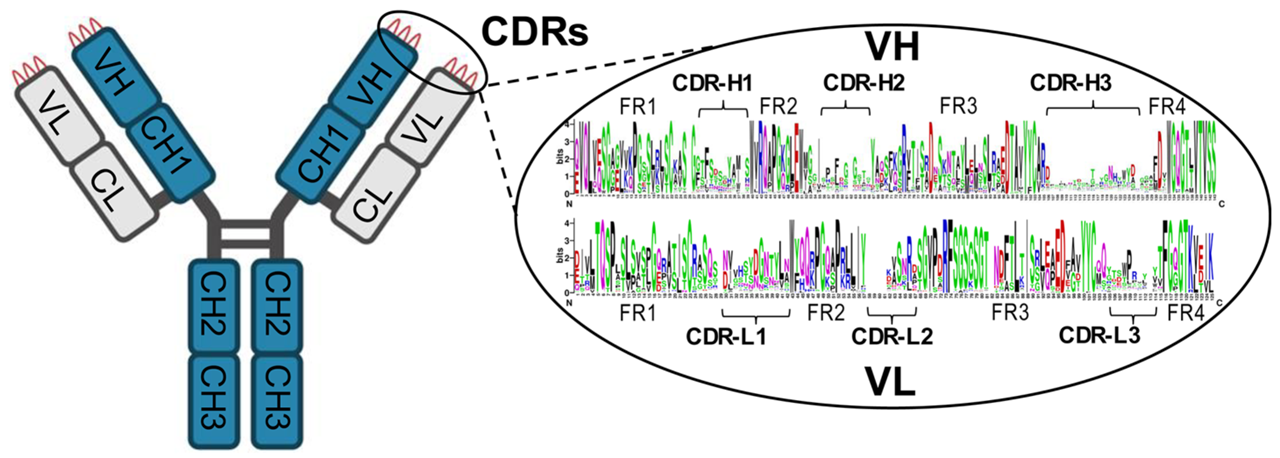
图 4 利用质谱对多克隆抗体进行表征和测序面临的挑战
免疫亲和蛋白质组学解锁T细胞免疫评估的新维度
免疫亲和蛋白质组学为T细胞免疫评估提供了一种突破性的方法:通过IA-MS鉴定MHC呈递肽段,构建MHC肽段复合物(pMHC),裂解细胞并富集pMHC特异性TCR,再通过质谱进行定量,从而实现对T细胞的精准检测(图5)。不过,该方法也面临一些挑战,如HLA等位基因的多样性、pMHC-TCR的低亲和力以及无法区分活/死细胞等问题。未来,随着技术的不断发展,有望通过pMHC富集特定的TCR,并进行从头测序,为CAR-T等免疫治疗疗法提供支持,彻底革新细胞免疫评估与精准治疗范式。
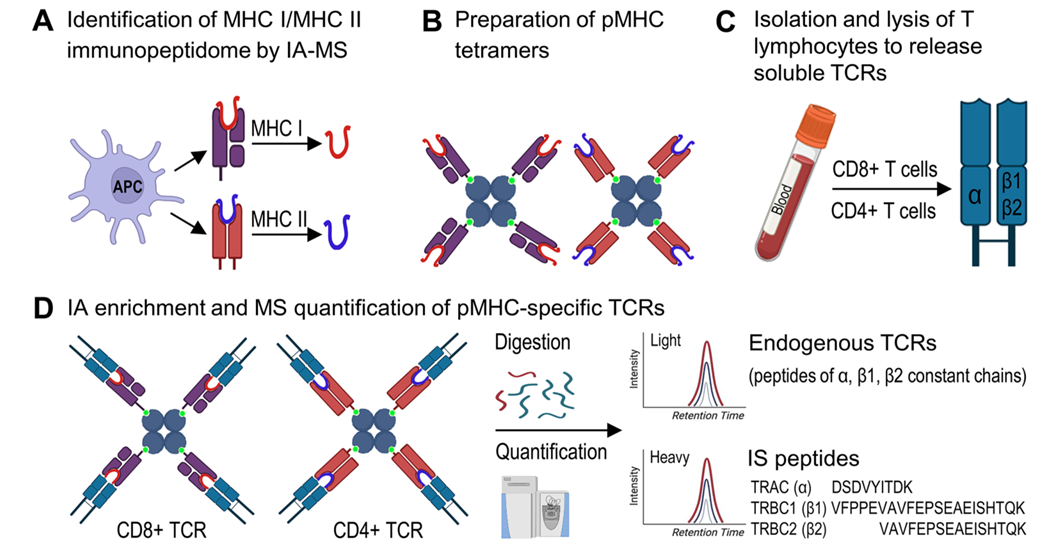
图 5 体外分析pMHC特异性TCR的IA-MS工作流程示意图
关注点:
(1)本文详细介绍了不同血清学分析方法的优缺点,其中基于质谱的方法在血清学诊断、新抗原鉴定、抗体测序等领域具有极大的应用价值。
(2)文中提及质谱技术在多发性骨髓瘤(MM)患者M蛋白检测中的价值,Rapid Novor 快序生物基于成熟的质谱和从头测序技术,开发了EasyM项目,实现MM患者M蛋白的微小残留病灶(MRD)检测,现已拿到美国CLIA认证,可为患者和药企提供服务[2]。
(3)这篇在2023年发表的综述中,介绍了血清多抗测序的难点和在抗体开发、疗法拓展、精准免疫学研究等领域的应用前景,这也是该技术被誉为抗体开发技术“圣杯”的重要原因。Rapid Novor快序生物于2024年10月在Nature子刊发文,全球首次报道了对人血清多抗的直接测序,并成功获得B细胞测序遗漏的高价值新冠中和抗体,标志着这项技术已经成熟[3]。
(4)文中也指出质谱技术在MHC结合肽段鉴定中的应用价值。Rapid Novor快序生物基于质谱和从头测序技术开发的新抗原鉴定服务,可一网打尽不同突变来源的新抗原,为免疫疗法开发提供助力。
参考文献:
[1]Walter J, Eludin Z, Drabovich AP. Redefining serological diagnostics with immunoaffinity proteomics. Clin Proteomics. 2023 Oct 12;20(1):42. doi: 10.1186/s12014-023-09431-y. PMID: 37821808; PMCID: PMC10568870.
[2]Fan H, Wang B, Shi L, Pan N, Yan W, Xu J, Gong L, Li L, Liu Y, Du C, Cui J, Zhu G, Deng S, Sui W, Xu Y, Yi S, Hao M, Zou D, Chen X, Qiu L, An G. Monitoring Minimal Residual Disease in Patients with Multiple Myeloma by Targeted Tracking Serum M-Protein Using Mass Spectrometry (EasyM). Clin Cancer Res. 2024 Mar 15;30(6):1131-1142. doi: 10.1158/1078-0432.CCR-23-2767.
[3]Le Bihan T, Nunez de Villavicencio Diaz T, Reitzel C, Lange V, Park M, Beadle E, Wu L, Jovic M, Dubois RM, Couzens AL, Duan J, Han X, Liu Q, Ma B. De novo protein sequencing of antibodies for identification of neutralizing antibodies in human plasma post SARS-CoV-2 vaccination. Nat Commun. 2024 Oct 10;15(1):8790. doi: 10.1038/s41467-024-53105-8. PMID: 39389968.