
在生物制药领域,临床开发阶段的居高不下的淘汰率极大地增加了项目平均投资成本。因此,在药物研发的早期评估其可开发性就显得尤为关键。可开发性涵盖了众多因素,如抗体来源、生物物理和药代动力学特性、重组表达效果等。这些因素相互交织、共同作用,综合决定了一个分子能否顺利开发成安全有效的药物。本文围绕早期可开发性评估,介绍了关键指标,以及针对这些指标的评估和优化方法流程,为降低药物研发的失败率,提升生产质量,并削减生产成本提供参考。
抗体的来源
抗体是生物制剂中最大的一类,其来源和序列起源都会影响其可开发性。天然抗体通常取自免疫后的动物或患者群体,由于在体内经历了亲和力成熟和自身耐受过程,通常具有良好的可开发性。然而,非人源抗体可能引发严重的免疫反应,需要进行人源化改造,或者使用转人免疫球蛋白基因的动物进行免疫。近年来,合成抗体受到越来越多的关注。理论上,它能够针对任何靶标筛选出结合物。借助体外展示技术,科研人员能对抗体库进行精准控制,例如剔除不利于结合的氨基酸残基、调整可变区长度等。不过,合成抗体也存在一些问题,由于其未经过体内成熟过程,且并非源自天然,可能出现多反应性、免疫原性、易聚集性以及表达特性不佳等情况。
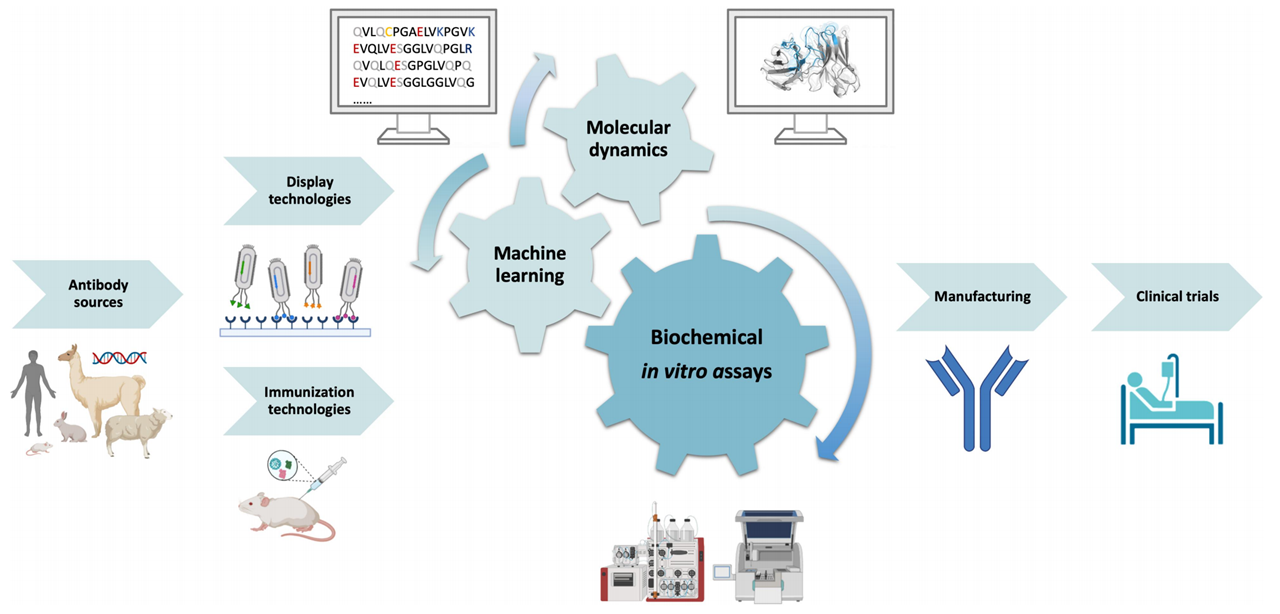
图1 生物药物研发的可开发性评估流程
展示技术的进展
过去几十年,展示技术发展迅速,使得构建庞大且多样的抗体、蛋白质和多肽群体,并从中分离出具有特定靶标结合特性的分子成为可能。然而,仅专注于提高亲和力对先导抗体进行工程改造,可能会产生亲和力增强但生物物理特性更差的分子。抗体在高浓度配方中的聚集倾向、非特异性相互作用程度以及药代动力学特性等因素,都可能导致开发失败。如今的展示技术也可实现对生物物理特性的筛选。例如,噬菌体展示技术可用于筛选高热稳定性克隆,哺乳动物展示系统则能筛选高浓度下稳定的克隆。多参数流式细胞术能在保留抗原结合能力的同时,筛选生物物理特性。
生物物理特性表征
在抗体开发时,通常要在数十到数千个候选抗体中筛选出唯一的一个进行后续研究,因此生物物理特性表征在筛选候选抗体时至关重要。理想的抗体药物需要具备高特异性、高胶体稳定性和低聚集倾向以及高折叠稳定性。常用于非特异性结合评估的方法有ELISA、多特异性粒子(PSP)检测、色谱法等。检测抗体自身相互作用的方法包括自相互作用色谱法(SIC)、交叉相互作用色谱法(CIC)等。由于抗体制剂的目标是在几年内稳定,因此为加快稳定性分析,常采用各种应激条件。热稳定性是一个关键指标,通常使用差示扫描量热法或差示扫描荧光法进行测量。除此外,疏水纳米颗粒表面介导的应激也可用于评估抗体稳定性。
数据、机器学习与可开发性的计算评估
在抗体开发的早期阶段,通常缺乏实验数据,此时计算评估就发挥了重要作用(图2)。通过对抗体序列和结构的分析,可以预测其开发性特性。例如,通过检测化学降解基序、糖基化基序以及预测潜在的聚集倾向区域和MHC II结合免疫表位等,帮助筛选出更具开发潜力的抗体。机器学习方法的应用,进一步提升了计算评估的能力。它可以从抗体序列中推断开发性参数,甚至生成具有特定特性的新抗体序列。不过,目前该技术仍面临一些挑战,如需要大量的训练数据,以及如何确保生成的抗体序列具有实际应用价值等问题。
从结构和分子动力学看生物制剂的生物物理特性
抗体的三维结构始终处于持续波动的状态,仅依靠单一的静态结构,通常无法全面阐释抗体的功能与特性。因此,将抗体的互补位描述为溶液中的构象集合更为恰当。例如,研究表明抗体的聚集现象会因低丰度状态而加速,抗体与表面发生疏水相互作用时,其构象会朝着更疏水的状态转变,这种转变使得抗体更容易聚集(图2A-B)。分子动力学模拟能够提供溶液中的构象集合,呈现与疏水、聚集等相关的构象情况(图2C-D)。
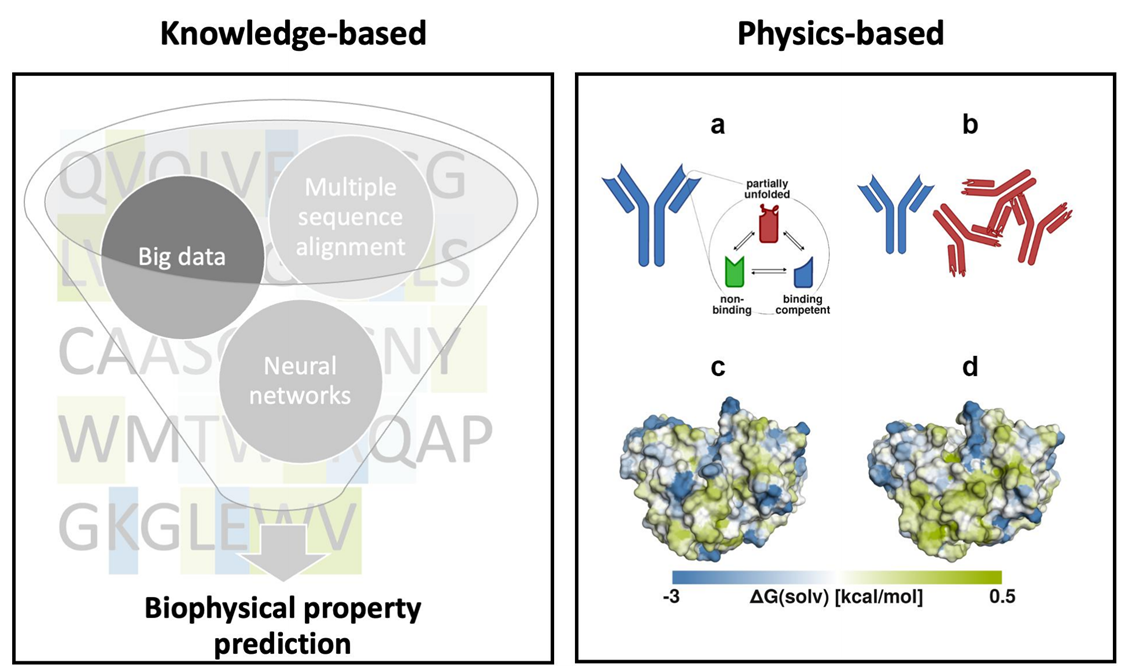
图2 基于知识和物理的方法在表征抗体生物物理特性方面的应用
细胞和动物模型用于可开发性评估
细胞检测方法也是评估可开发性的重要手段。治疗性生物制剂可能具有免疫原性,引发多种问题。外周血单个核细胞(PBMC)免疫激活检测可用于检测激活T细胞的表位,但生物制剂在患者体内的免疫原性仍难以预测(图3)。
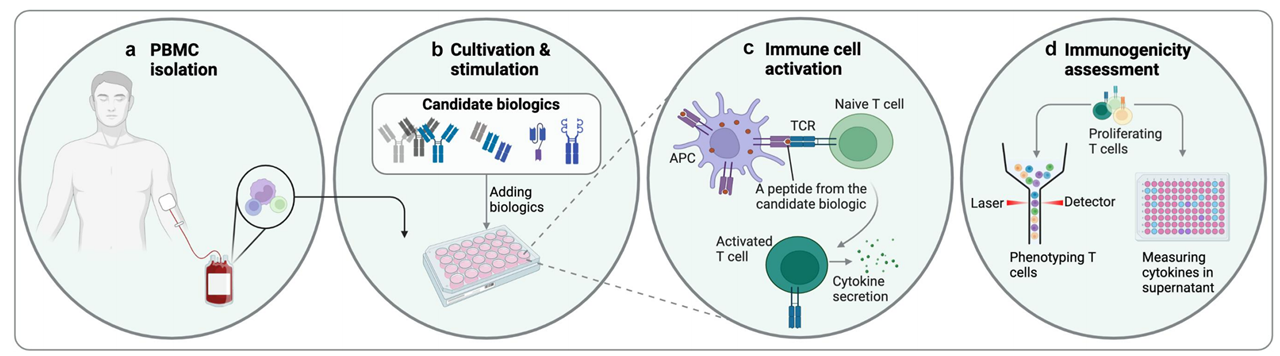
图3 PBMC免疫原性检测
IgG和相关药物能与新生儿Fc受体(FcRn)结合,影响其药代动力学特性。人内皮细胞再循环检测(HERA)可用于评估FcRn靶向分子的摄取和再循环能力,预测其体内特性,且细胞检测结果与体内数据有较好的相关性(图4)。
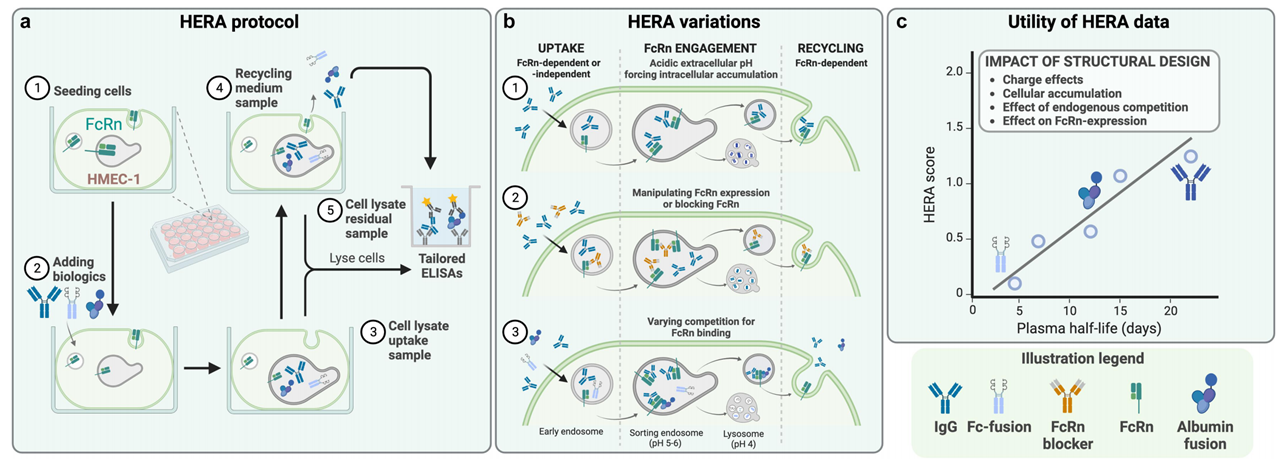
图4 HERA用于体外药代动力学和FcRn靶向策略研究
在临床前药代动力学评估方面,小鼠由于成本和伦理等优势成为常用动物模型,但在使用时要考虑跨物种差异。人FcRn转基因小鼠是评估人IgG生物制剂药代动力学的金标准,但小鼠内源性IgG水平低等因素会影响研究结果,可通过预静脉注射高浓度IgG或使用特定转基因小鼠来解决。
生物制剂的生产与应用
生物制剂的细胞系开发与生产同样不容忽视,要以高效、安全且可重复的方式生产生物制剂。目前,哺乳动物细胞凭借其能够正确进行蛋白质折叠、糖基化修饰等复杂翻译后加工过程的优势,成为生产抗体治疗药物的常用选择,但也面临细胞培养过程复杂等挑战。目前,大多数生物制剂通过注射给药,但口服给药等替代途径也在积极探索中。对于口服生物制剂,其在胃肠道中的稳定性和货架期等成为关键开发性因素。
总结
生物制剂的早期开发性评估,是一个多维度、综合性的复杂过程,贯穿从抗体来源筛选,到临床应用的各个环节。随着技术的不断进步,包括展示技术、生物物理特性评估方法、计算评估工具以及细胞分析和动物模型的优化,生物制剂的开发将变得更加高效、精准,为患者带来更多安全有效的治疗选择。
关注点:
(1)来源于免疫后人或动物的天然抗体,在体内经历了亲和力成熟和自身耐受过程,因而往往具有良好的可开发性,然而传统抗体筛选方法,难以直接获得循环抗体的序列。
(2) Rapid Novor快序生物全球唯一的多抗测序技术,可以直接对人或动物血清多抗蛋白测序,高效获得与原始多抗性能相当的优质天然单克隆抗体序列,其可开发性更高。
参考文献:
[1]Fernández-Quintero ML, et al. Assessing developability early in the discovery process for novel biologics. MAbs. 2023;15(1):2171248. doi:10.1080/19420862.2023.2171248