在生物学研究和医学诊断领域,血清学检测意义重大,它通过测量生物样本中的特异性抗体,助力监测疫苗效果、诊断疾病、了解病毒传播动态等。然而,传统血清学检测方法如ELISA,每次只能对单个样本的一种抗原进行检测,耗时费力,成本又高。开发高通量、灵敏的免疫诊断方法能够改善血清学检测的现状。本文中,研究团队开发出基于质谱流式分析同位素编码微珠的高通量多重血清学检测技术,为该领域带来新突破。
质谱流式细胞术作为一种质谱分析、多参数单细胞技术,在过去十年中被广泛用于细胞分析。它使用金属同位素标记抗体,借助高分辨质谱精准区分,解决了荧光通道的串色问题。该技术通常可对细胞分析超50个参数,通道重叠极少。以38通道为例,其可编码的空间可达数十亿种。基于上述优势,质谱流式特别适合用于高通量血清学检测。本文研究团队建立了一种实用、低成本且高度可扩展的基于微球和质谱流式的多重血清学检测方法。他们通过聚苯乙烯微球负载同位素,构建了含18480种组合的编码空间,采用质谱流式细胞术进行定量分析。在实际案例中,一名操作人员不用自动化设备,8小时就能完成924个临床血清和血浆样本的SARS-CoV-2相关抗体检测。
同位素标记微球的策略
通过质谱流式细胞术实现基于微球的高通量检测,需满足两个条件:(1)每个微球均匀掺入高负载量的同位素;(2)可生成大量同位素编码微球。研究人员将与同位素偶联的生物素化蛋白和链霉亲和素包被的聚苯乙烯微球相结合,实现微球均一高负载同位素(图1 a)。例如将稳定同位素镝162(162Dy)与生物素化牛血清白蛋白(BSA)偶联,负载到链霉亲和素包被的微球上,经质谱流式分析表明每个微球负载量高且均一(图1 b)。随后,使用该策略共构建了38种同位素微球(图1 c)。
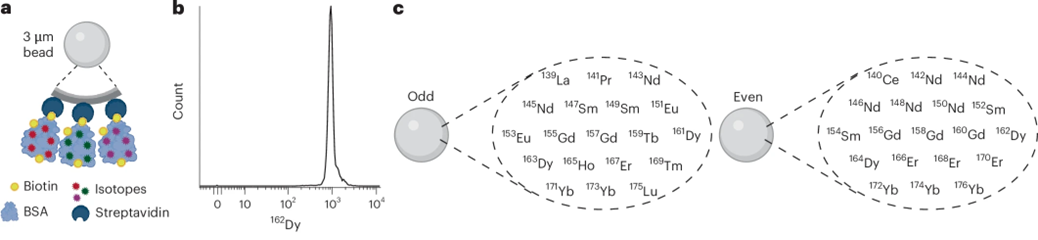
图1 聚苯乙烯微球合成后掺入稳定同位素的策略
一种高通量创建数千个同位素编码聚苯乙烯微球的策略
高通量血清学检测应用涉及两个主要部分:一是分析单个样本多个分子靶点的能力,二是分析大量样本的能力。为解决这些问题,团队设计了一种双重编码策略,每个微球含两组同位素:一组识别分子靶点,另一组识别样本。每个微球先在6种同位素中负载3种,生成20种组合,再在其他12种同位素中负载6种,生成924个编码。利用18种同位素,团队共创建了18480个编码(图2 a)。之后,团队开发了自动解码流程,可以准确解码两层编码(图2 b c),且18480个编码的回收率达到了100%。
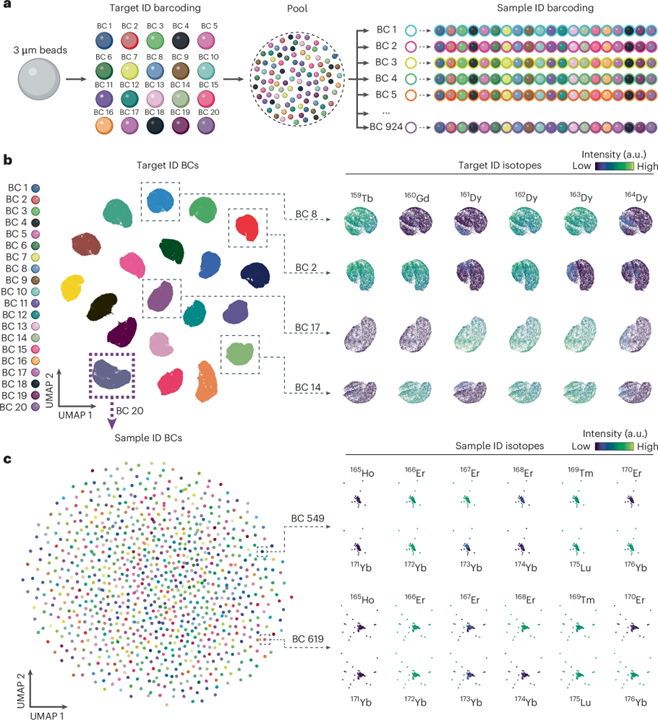
图2 双重编码策略实现了18480种同位素编码微球的生成
一种使用少量样本检测血浆抗体的检测方法
接下来,团队首先展示了这个系统在少量样本分析中的应用(图3 a)。此系统中,一个微球用预定义的同位素编码,并负载生物素化抗原;另一个磁性微球与抗人免疫球蛋白偶联。只有在存在识别目标抗原的抗体时,编码微球才与磁性微球发生交联。利用磁铁吸附交联微球,通过质谱流式分析流出液与基线微球混合物中的微球计数之比,以此估计宿主抗体水平,比值低表明样本中有针对该抗原的宿主抗体。
在成功构建这套系统后,团队将它应用于SARS-CoV-2的检测。通过将负载有SARS-CoV-2刺突蛋白S1亚基的编码微球与稀释300倍的新冠康复者或阴性对照者血浆孵育。质谱流式结果表明,SARS-CoV-2康复者血清中微球数量减少,表明其体内抗体的存在(图3 b c)。通过ELISA检测上述血清的结果表明,除两份样本外,所有的SARS-CoV-2康复者样本都有S1结合能力(图3 d)。
随后,团队利用同位素微球广泛的编码空间,分析了39个SARS-CoV-2阳性个体和55个新冠前阴性个体的血浆样本。在这个案例中,按照1:300,1:3000,1:30000对样本进行梯度稀释,相当于在30μl体系中使用100 nl,10 nl或1 nl样本。分别负载SARS-CoV-2 刺突蛋白S1亚基、刺突 S1受体结合区域(RBD)、刺突蛋白S2亚基和核衣壳蛋白的编码微球,在100 nl样本量下能100%识别出新冠患者样本,部分样本仅通过1 nl即可检测到抗S1的抗体(图3 e)。对每个样本的十二次检测中均得到类似的结果,表明该方法检测可靠(图3 f)。此外,该分析也发现了不同个体对于SARS-CoV-2抗体谱存在个体差异(图3 e)。这些数据表明,双微球策略可以在低至1纳升的少量样本中检测到宿主抗体,并且可以呈现患者针对多种抗原的独特抗体反应谱。
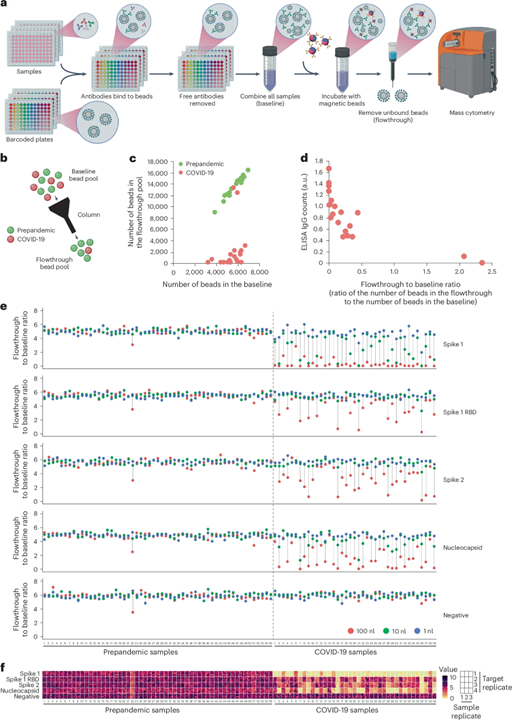
图3 用于在少量血浆中检测特异性抗体的双微球策略
一种用于多重抗体检测的高通量、免洗检测方法
研究团队设计了一个包含连续固定和变性的免洗系统,以解决传统血清学检测中繁琐的洗板流程的问题(图4 a)。首先将负载抗原的同位素编码微球与样本一起孵育,与宿主抗体结合,然后用多聚甲醛(PFA)将宿主抗体固定在微球上。再用十二烷基硫酸钠(SDS)处理,使抗体蛋白变性,同时确保不会使微球上的同位素脱落,然后将所有样本混合并洗涤,之后将样本与同位素标记的二抗孵育,最后通过质谱流式分析,以检测每个编码微球上结合的宿主抗体。
为了展示这一系统用于大规模多重血清学检测的能力,研究团队分析了542份SARS-CoV-2感染者血清中19种SARS-CoV-2变体的抗体IgG和IgM水平(图4 b c)。整个队列中,抗野生型SARS-CoV-2三聚体蛋白IgG水平随着时间的推移而升高(图 4d)通过质谱流式细胞术得到的针对野生型SARS-CoV-2三聚体蛋白的IgG水平,与使用对照检测方法检测得到的结果相关性良好(图 4e)。
该检测为同一样本的多个靶点提供内部对照数据,可比较同一个体对不同SARS-CoV-2的抗体反应。多数样本针对SARS-CoV-2变体的抗体反应相关性高,但部分样本对某些变体反应独特,可能反映了由患者或病毒相关因素引起的抗体库差异(图 4f)。这些数据表明,基于微球的质谱流式多重血清学检测是定量的、灵敏且特异的,与现有诊断方法相比,可扩展性极大提升。该方法可在30微升的反应体积中,使用400纳升的样本体积,在一支试管中进行36960次检测。
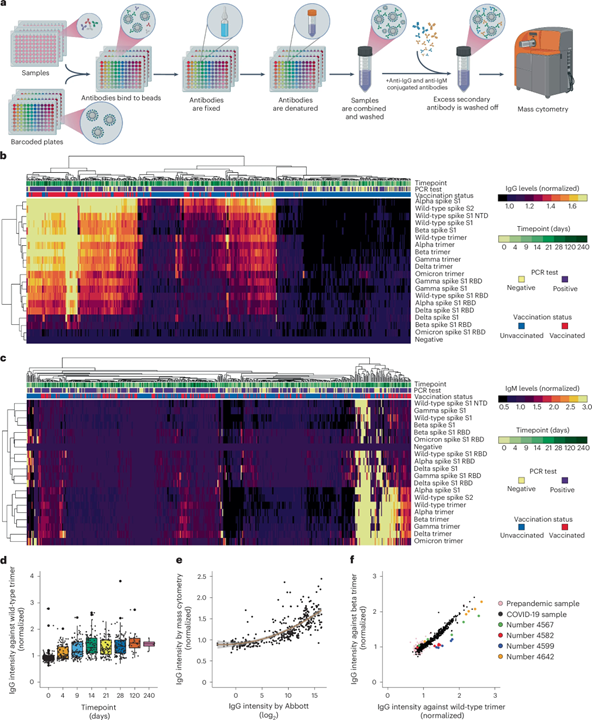
图 4 一种用于多重抗体检测的高通量免洗策略
关注点:
1、本研究建立了一种基于同位素编码微球的高通量多重检测策略,可以用于大规模多重血清学检测。不仅适用于抗体检测,也适用于抗原检测。
2、质谱流式技术对抗体的特异性、亲和力、稳定性等特征提出了更高要求,也对现有抗体发现技术提出了更高挑战。
3、Rapid Novor 快序生物可提供全球唯一从人或动物血清多抗出发的抗体开发路径,直接获得可开发性更高的天然抗体。
参考文献:
[1] Drainas AP, McIlwain DR, Dallas A, Chu T, Delgado-González A, Baron M, Angulo-Ibáñez M, Trejo A, Bai Y, Hickey JW, Lu G, Lu S, Pineda-Ramirez J, Anglin K, Richardson ET, Prostko JC, Frias E, Servellita V, Brazer N, Chiu CY, Peluso MJ, Martin JN, Wirz OF, Pham TD, Boyd SD, Kelly JD, Sage J, Nolan GP, Rovira-Clavé X. High-throughput multiplexed serology via the mass-spectrometric analysis of isotopically barcoded beads. Nat Biomed Eng. 2025 Feb 12. doi: 10.1038/s41551-025-01349-0.