1型糖尿病(T1D)是一种自身免疫性疾病,其特征是胰岛中效应T细胞的过度激活会清除自身的胰岛β细胞,最终导致胰岛素的严重不足。目前,胰岛素是唯一获准用于治疗T1D的主要疗法。尽管胰岛素能够维持患者的生命,但这种治疗方式要求患者进行规律的注射和长期的用药,对患者及其家庭构成了沉重的心理和经济压力。
1型糖尿病存在的自身免疫问题仍然有待解决。既往的免疫治疗方案受限于免疫抑制作用或者疗效期短等问题。近期临床试验转向一种新的治疗方法——使用调节性T细胞(Tregs)来治疗1型糖尿病。Treg细胞在抑制自身免疫反应方面发挥着关键作用,而这种抑制能力的下降与多种自身免疫疾病的发生紧密相关,T1D也在其中。被诊断为T1D的患者通常会出现Treg数量减少或功能缺失的现象。因此,Treg细胞也引发了科学家的兴趣,他们正在进行相应的临床试验。
Treg疗法在治疗T1D方面仍处于起步阶段。目前,Treg细胞的治疗效果和特异性尚未完全满足临床应用的高标准和安全性要求,因此还需要进一步优化。南达科他大学研究团队给Treg细胞表达了嵌合抗原受体(CAR),使其能识别来自胰岛的内分泌细胞(包括β,α,δ和PP细胞),抑制T细胞对胰岛β细胞的损伤,从而解决了上述问题。这种CAR的核心是一个单链可变片段(scFv),靶向内分泌细胞的表面标志物HPi2。研究团队使用了快序生物(Rapid Novor)的REmAb单克隆抗体从头测序服务准确地测定了抗HPi2抗体的可变区序列,进而将这些序列应用于HPi2-CAR scFv的设计中。
不难看出团队使用的从头测序技术给CAR T细胞疗法带来了极大地便利。蛋白从头测序可以为CAR的设计、构建和验证提供支持,从而简化了靶点的识别和筛选过程。该过程包括对靶点已知的抗体进行测序,进而利用所得的抗体序列来构建CAR的铰链区和抗原结合域。掌握了这些关键的序列信息后,就能对治疗方案进行深入的优化,以期望达到更为理想的治疗效果。
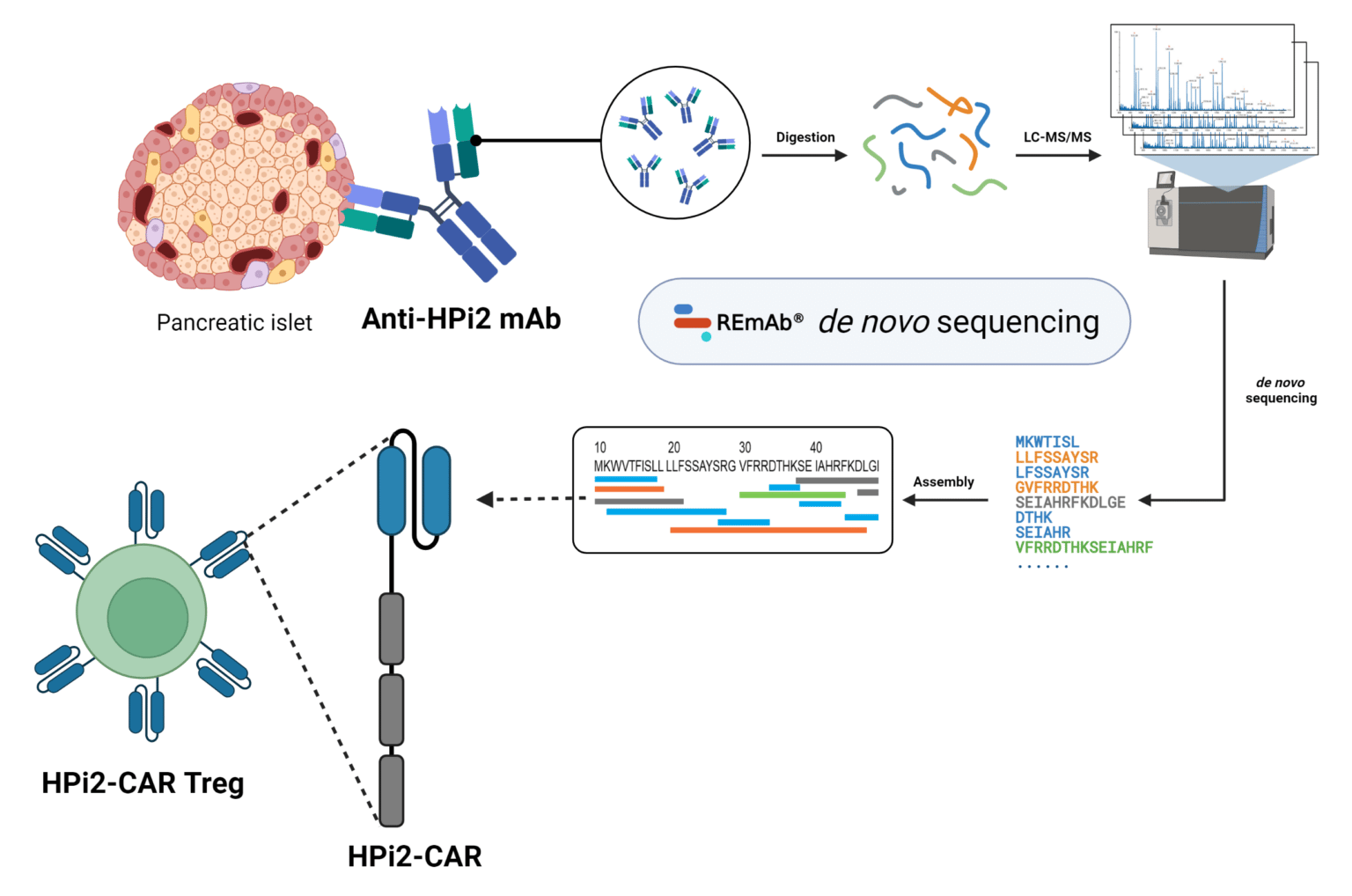
HPi2-CAR Treg的改造流程,使用Rapid Novor的REmAb服务对抗HPi2抗体进行从头测序。
关注点:
1. 南达科他大学研究团队利用蛋白从头测序技术获得了抗HPi2抗体序列,用于HPi2-CAR的设计、构建和验证。
2. 获得完整的抗体序列为CAR的结构组成和设计提供重要信息,这不仅有助于优化治疗方案,还能显著加速细胞治疗的研发进程。
参考文献:
Radichev IA, Yoon J, Scott DW, Griffin K, Savinov AY. Towards antigen-specific Tregs for type 1 diabetes: Construction and functional assessment of pancreatic endocrine marker, HPi2-based chimeric antigen receptor. Cell Immunol. 2020;358:104224. doi:10.1016/j.cellimm.2020.104224