
KRAS,这个在人类癌症中突变频率居高不下的致癌基因,曾长期被贴上“不可成药”的标签,困扰全球科研界数十年。直到近年来,KRASG12C共价抑制剂的问世,才终于打破这一僵局。然而,临床实践很快抛出新的难题:尽管这类药物初期疗效显著,耐药性却如影随形,多数患者在用药一年内便会出现疾病进展,陷入“靶向有效却难持久”的困境。
耐药后该怎么办?传统治疗思路多聚焦于开发下一代抑制剂,但KRAS耐药机制复杂多样——可能是KRAS信号通路持续激活,可能是旁路通路异常激活,也可能是KRAS基因扩增。幸运的是,研究人员发现一个关键线索:KRASG12C突变中的半胱氨酸残基本身,很少发生二次突变。这意味着,即便肿瘤产生耐药,G12C突变依然会保留在癌细胞中,理论上仍是可靶向的“靶点”,核心问题在于:如何精准捕捉并利用这个靶点,清除耐药癌细胞?
近期,发表在国际顶级期刊《Nature Communications》上的一项重磅研究,为破解这一困局提供了全新的思路。来自Aethon Therapeutics的研究团队首次通过质谱免疫肽组学技术,直接定量了KRASG12C抑制剂在肿瘤细胞表面“创造”的独特“合成新抗原”,并通过工程化抗体将其牢牢“锁定”,引导人体免疫系统精准清除耐药肿瘤细胞。这一突破不仅为KRAS抑制剂耐药患者提供了强有力的治疗武器,更开创了“合成新抗原”免疫治疗的全新范式,为肿瘤精准治疗开辟了新赛道。
一、 KRASG12C:从突破“不可成药”到陷入耐药困局
KRAS基因就像是细胞生长的“开关”,正常情况下,它能精准调控细胞的增殖与分化。然而,当它发生突变时,这个开关就会被卡在“开启”状态,导致细胞不受控制地疯狂生长,最终癌变。在所有KRAS突变中,G12C突变是其中一种重要的亚型,它在非小细胞肺癌、结直肠癌和胰腺癌等多种恶性肿瘤中均有发生,仅在美国,每年就有数万名新确诊患者携带这一突变。
2021年,全球首款KRASG12C抑制剂Sotorasib的获批,标志着人类终于攻克了KRAS“不可成药”的历史难题。这类药物能精准地插入突变KRAS蛋白的特殊口袋,共价结合并关闭其活性,从而抑制肿瘤生长。但临床数据显示,尽管大部分患者在治疗初期肿瘤显著缩小,约一半的患者在一年内就会对药物产生耐药性。更棘手的是,耐药后的肿瘤细胞往往依然保留着G12C突变,这意味着它们依然是“罪魁祸首”,却对原有的靶向药不再敏感。
如何清除这些耐药的肿瘤细胞?科学家们将目光投向了人体自身的免疫系统。如果能让免疫细胞识别并杀死这些“顽固分子”,或许就能打破耐药困局。
二、 质谱首次直接定量靶向药创造的“人造新抗原”
在此之前,学术界通过间接证据推测KRASG12C抑制剂会形成带修饰的p*MHC新抗原。研究团队通过质谱免疫肽组学技术,搭配稳定同位素标记内标肽,首次直接鉴定了sotorasib、adagrasib、divarasib三种临床常用KRASG12C抑制剂修饰的新抗原。
实验结果明确:sotorasib修饰的soto-p7肽是核心靶抗原,可呈递在HLA-A3超型分子(A03:01、A11:01、A68:01)表面。但这个靶点存在两大致命缺陷:
丰度极低:在人工构建的KRAS/HLA过表达细胞系中,soto-p7的丰度仅约10拷贝/细胞;而在临床相关的内源性肿瘤细胞中,其丰度低于1拷贝/细胞。
稳定性极差:soto-p7在A03:01上的半衰期仅约30分钟,在A*11:01也仅约90分钟,远低于野生型p7肽。也就是说,这个新抗原刚被送到细胞表面,很快就会降解消失,根本来不及被免疫细胞识别。
这一结果既证实了药物修饰合成新抗原的真实存在,也直指后续研发的核心方向:必须提升新抗原的稳定性与表面密度。
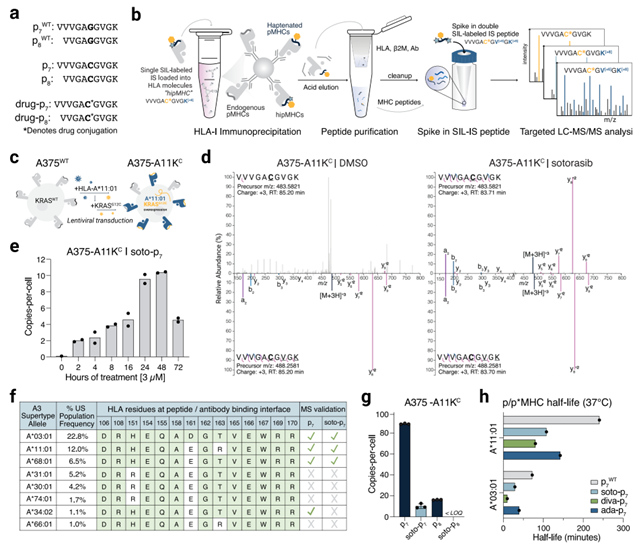
图1 质谱鉴定HLA-A3呈递的药物修饰KRASG12C肽段
三、AETX-R114:让不稳定的新抗原“站稳脚跟”,精准杀伤耐药癌细胞
既然抗原不稳定、丰度太低,能不能想办法把它“稳住”?研究团队基于冷冻电镜结构指导,对先导抗体R023进行精准亲和力成熟,聚焦轻链互补决定区(CDR)改造,最终筛选出p*MHC高亲和力抗体R114,并将其与抗CD3效应臂融合,构建出半衰期延长的双特异性T细胞衔接器(TCE)——AETX-R114。
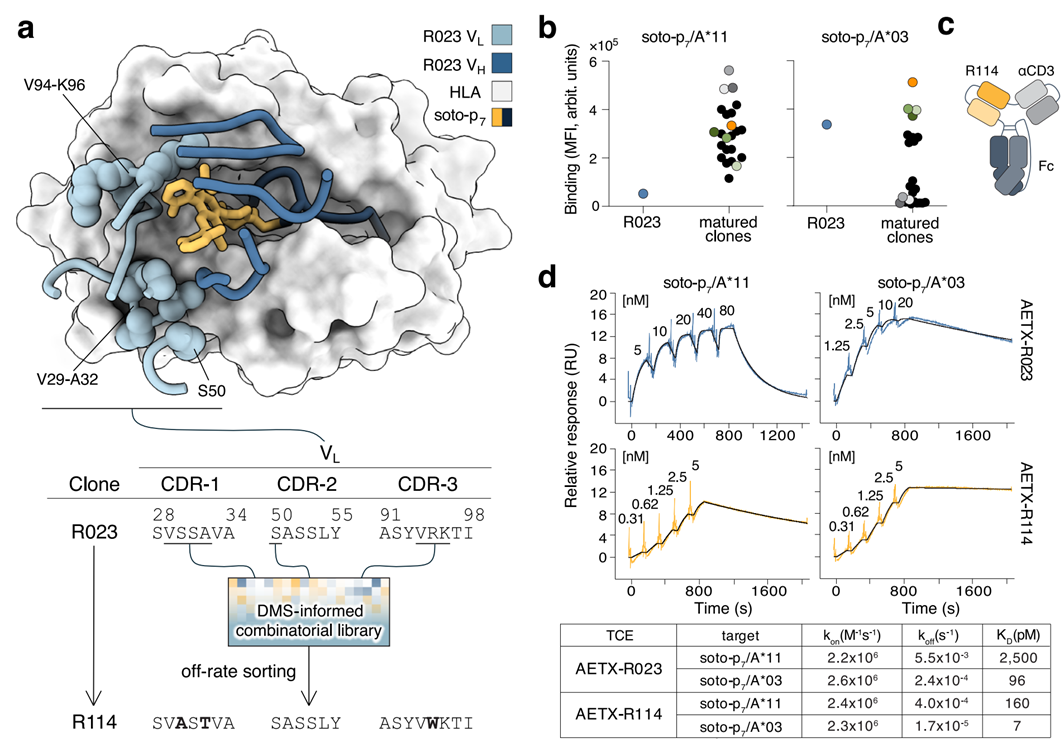
图2 亲和力成熟抗体AETX-R114 的开发与结合特性
实验结果表明,通过抗体介导的稳定作用,成功逆转了抗原的不稳定性:将p*MHC半衰期从30/90分钟,延长至24小时以上,使NCI-H2122内源性肿瘤细胞表面抗原密度从不到1拷贝/细胞提升至14拷贝/细胞,让原本低丰度、稍纵即逝的“人造新抗原”,终于能稳稳“站”在癌细胞表面,成为免疫治疗的可用靶点。
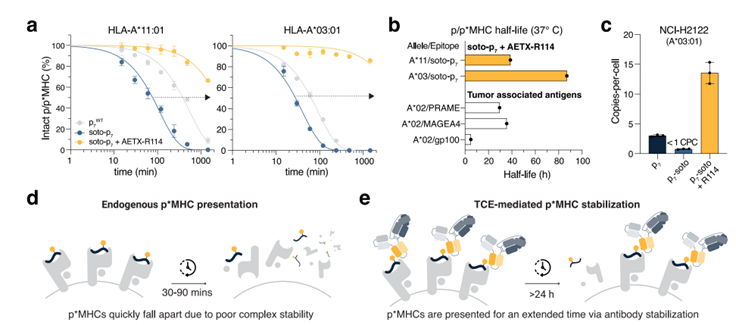
图3 抗体增强Soto‑P7的表面表位密度
进一步的体内外药效实验表明,AETX-R114仅在KRASG12C抑制剂存在时,高效激活CD8+T细胞、促进IFNγ分泌,特异性杀伤耐药癌细胞,且显示出了良好的安全性。
四、AETX-R302:突破HLA限制,覆盖更广人群
为进一步扩大适用人群,研究团队又继续开发了靶向divarasib修饰KRASG12C新抗原的AETX-R302。令人惊喜的是,R302不仅能识别HLA-A3超型,还能识别HLA-A*02:01,理论上可覆盖美国人群中66%的基因型(AETX-R114覆盖39%)。
体外实验显示,AETX-R302对HLA-A02:01、A03:01、A11:01均具有纳摩尔级亲和力,在人工肽段脉冲实验中可介导T细胞跨超型杀伤。但在药物处理的内源性肿瘤细胞中,目前仅观察到对HLA-A11阳性细胞的有效杀伤——因为diva-p7在A02和A03上的稳定性太差,无法达到有效呈递水平,这也是后续优化的核心方向。
冷冻电镜结构解析揭开了跨超型识别的核心机制:R302识别表位同时包含HLA分子、药物半抗原和肽段三部分,不同长度的肽段通过构象偏移,使药物半抗原处于完全相同的空间位置,被R302精准识别。此外R302的CDR-H3 N端采用了罕见的'LY'序列,而非合成抗体文库中常见的'AR'序列。这是其独特结合界面的关键决定因素之一,为跨HLA超型识别提供了重要结构基础。
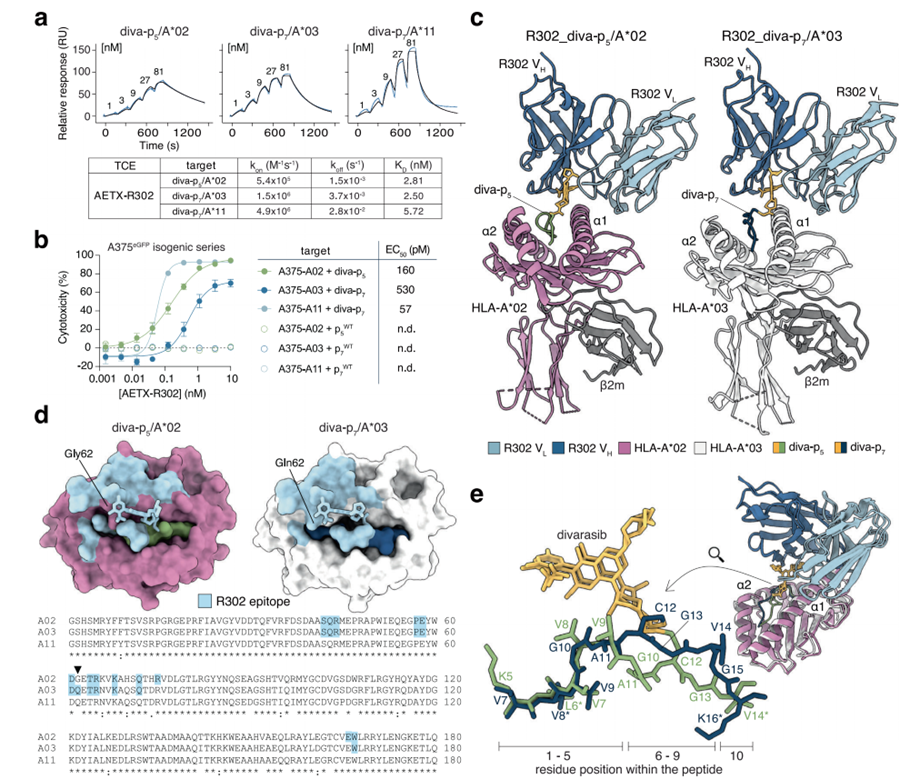
图4高亲和力、跨HLA超型抗体R302的功能与结构表征
五、临床价值:开创合成新抗原免疫治疗新范式
这项研究的意义远不止针对KRASG12C单一靶点,更开创了“共价抑制剂+合成新抗原+工程化抗体”的全新免疫治疗范式,破解了肿瘤免疫治疗的多个核心痛点:
盘活不可靶向的胞内致癌靶点:KRAS、EGFR、BTK等多数致癌靶点位于细胞内,传统抗体无法触及。而共价抑制剂可将其转化为表面p*MHC新抗原,让胞内靶点变成免疫治疗靶标;
解决低丰度、不稳定抗原难题:高亲和力慢解离抗体可稳定并富集不稳定/低丰度的新抗原,让原本无法成药的靶标变得“可靶向”;
扩大适用人群:跨超型抗体无需对不同HLA亚型进行个体化定制,大幅降低了“现货型”免疫疗法的开发成本;
直击耐药困境:由于KRASG12C耐药细胞依然保留G12C突变,该疗法有望对一线靶向药耐药患者依然有效,有效地填补后线治疗空白。
结语
从KRAS“不可成药”的绝望,到共价抑制剂的突破性问世,再到合成新抗原免疫治疗的全新突破,KRASG12C突变癌症的治疗历程,正是人类与癌症不懈抗争的缩影。本研究用质谱技术精准鉴定新抗原靶点,用工程抗体“锁死”药物修饰新抗原,为解决KRASG12C耐药的临床痛点提供可行方案,更建立了可复制的精准免疫治疗新范式,未来有望为更多患者带来全新的治疗希望。
参考文献
Maso L, Mosure SA, Rodriguez-Aponte SA, et al. Engineered antibodies that stabilize drug-modified KRASG12C neoantigens enable selective and potent cross-HLA immunotherapy. Nat Commun. 2025;16(1):11264. Published 2025 Dec 17. doi:10.1038/s41467-025-66132-w