
单克隆抗体已成为了当今发展最为迅速的治疗药物之一。据预测,到 2028 年其全球销售额将达到 3466 亿美元。在抗体工程及研发领域的不断推进下,基于抗体的治疗药物结构变得愈发复杂精密(例如双特异性抗体和CAR-T)。近年来,随着高通量单 B 细胞测序以及血清抗体蛋白质组学方面的技术突破,直接从内源 B 细胞或循环抗体中鉴定出高亲和力抗体已成为现实。此外,人工智能领域的发展也为抗体发现和设计注入了强大动力。本文介绍了这些技术在抗体组库(antibody repertoire)分析中的应用进展及发展趋势。
抗体组库的组成
体液免疫的保护能力依赖于复杂且多变的抗体组库,这些抗体可以特异性识别抗原并介导免疫应答。B 细胞受体(BCR)是分泌型抗体的膜蛋白前体形式,每个B细胞产生一个独特的BCR。在抗原识别后,一部分 B 细胞可分化为浆细胞,主动分泌可溶性抗体,这些抗体能够结合病原体并促进其被清除。因此,个体的抗体组库被定义为完整BCR库以及分泌型抗体库的集合,它包含了两个在克隆和功能上有所不同但相互关联的部分(图1)。据估算,人类的抗体组库包含约 1015个独特序列,因此深入描绘这一复杂群体的全貌面临着极大的挑战。借助先进技术手段对抗体组库的转录、选择机制,以及抗原-抗体相互作用展开研究,将极大地加快抗体药物的研究、开发以及临床转化进程。

图1 人类抗体组库的分析。(左下)基于基因测序方法分析B细胞表达的BCR库;(左上)基于蛋白组学方法分析生物体液中的分泌型抗体库;(右方)人工智能(AI)工具加速抗体研发[1]
基于BCR测序的抗体组库研究
基于基因测序的抗体组库分析长期以来依赖第二代短读长平台(读长小于600个碱基对),例如由Illumina开发的测序仪是 BCR测序的金标准。目前发展的第三代长读长测序平台(如Pacific Biosciences 和 Oxford Nanopore Technologies)可提供更长的读长(大于1万个碱基对),随着其在准确性、通量以及成本降低方面取得的进展,正在逐步成为抗体组库分析的有力替代选择。例如,长读长测序可以分析不同个体之间免疫球蛋白重链(IGH)的基因组变异;可以可靠地对抗体进行同种型和亚型鉴定;还可以揭示在诸如癌症等各类病症中,抗体同种型亚型存在的偏好性。长读长测序可以提高轻重链可变区配对的准确性和可靠性,通过分析基因的使用情况和功能,可以发现不同疾病状态下的“公共抗体”,能够作为评估疫苗有效性的可靠生物标志物。
单细胞分析领域的技术突破使得大量的BCR库数据能够与基于多组学的各类数据集相整合。单细胞转录组学平台在剖析接种疫苗、感染以及自身免疫应答等情形下 B 细胞亚群之间的表型及功能差异方面发挥着关键作用。通过一项LIBRA-seq技术,可以结合抗原特异性评估和BCR测序。它利用流式细胞术分离出与带有荧光标记和条形码的抗原相结合的 B 细胞,通过测序获得它们的BCR序列,同时获得每个细胞相结合的抗原信息。对于不表达BCR的抗体分泌细胞(ASCs),通过一种名为TRAPnSeq的技术,可以在ASCs表面捕获其分泌的抗体,结合带条形码及荧光标记的抗原分选和单细胞测序,获得对应的抗原-抗体信息。整合功能筛选和BCR测序的各项技术发展,目前正推动以高通量的方式识别分泌型抗体库中具有功能的克隆,助力深入理解BCR特性、实现对适应性B细胞应答的精准调控。·
基于蛋白组学方法的免疫组库研究
尽管基于BCR测序的免疫组库研究已取得许多进展,然而不可忽视的是,外周血中存在的BCR并不能保证其会以分泌型抗体的形式存在。这一客观事实导致仅通过BCR测序不能深入了解血浆和黏膜分泌物中抗体的真实组成和丰度。随着蛋白质组学策略的进步,可以以全新的视角和方式,实现人体内抗体的特性、功能及作用靶点分析。
自下而上蛋白组学
自下而上蛋白质组学方法通过将抗体酶切成肽段,通过液质联用(LC-MS/MS)进行分析,与BCR测序数据库进行对比实现鉴定。该方法可以直接从多抗混合物中鉴定并定量数百种抗体谱系,但能否可靠地鉴定抗体谱系往往取决于能否检测到独特的互补决定区-H3(CDR-H3)肽段。这种传统的基于数据库比对的方法尽管已取得一定突破,但是在获得轻重链正确配对抗体的精准全长序列方面仍面临挑战。
自上而下和自中而下蛋白质组学
与自下而上蛋白质组学不同,自上而下方法不对蛋白进行酶切,而是将其直接通过LC-MS/MS进行分析,从而实现更好的序列覆盖度,改善抗体鉴定效果。然而完整抗体分子量较大(约150kda),且电荷数多,使得该方法面临重大挑战。目前该方法主要被用于高度纯化的单抗分析,例如糖基化、氧化、脱酰胺等分析。自中而下蛋白组学方法,是将抗体酶切成50-100 Kda的片段(Fab 或 F (ab’) 2),实现降低样本复杂程度,提高鉴定效率。该方法可以产生覆盖CDRs的碎片离子,从而保留轻重链可变区的配对信息。自上而下/自中而下蛋白质组学相结合的方法,能够对来自血浆的内源性抗体进行检测。通过结合这些方法,也有研究实现了单种血浆抗体的从头测序。
整合抗体序列、结构与特异性的计算工具
随着人工智能模型的发展,其为理解抗体-抗原相互作用提供了有力工具。但它们仍面临如CDRs结构预测、抗体-抗原相互作用、结合亲和力与中和活性优化、抗体可开发性等挑战。例如AlphaFold 2在单体蛋白质结构预测方面极为成功,而对多聚蛋白,如对抗体-抗原复合物预测成功率较低。除直接结构预测外,其他计算工具也被开发用于血清多抗中抗原特异性抗体的高分辨率结构表征,如从冷冻电镜图谱预测抗体序列的工具可预测抗体的特性及表位。随着冷冻电镜解析的抗体结构数量不断增加和人工智能技术发展,目前的计算模型已具备从头设计抗体的能力,但其优化依赖于整合全面理解抗体组库的数据。血浆抗体具备体内可分泌性、稳定性、溶解性、免疫原性最小化等特征,因此相关数据可为从头设计抗体提供有利信息并可能减少抗体开发过程中的瓶颈问题。
关键点
1. 对抗体组库的深入研究将助力抗体开发、增进免疫应答机制理解、促进人工智能技术在抗体研究领域中的应用。
2. 免疫组库由BCR和分泌型抗体,这两个在克隆和功能上不同但相互关联的抗体库组成,仅通过基因测序的方法无法洞察免疫组库的全貌。
3. Rapid Novor(快序生物)的REpAb(图2)是全球唯一实现直接对血清多抗测序,获得轻重链正确配对,经亲和力验证的抗体序列的技术,可以用于治疗性抗体发现、揭秘分泌型抗体库组成、促进对免疫组库的深入理解、助力抗体行业蓬勃发展[2]。
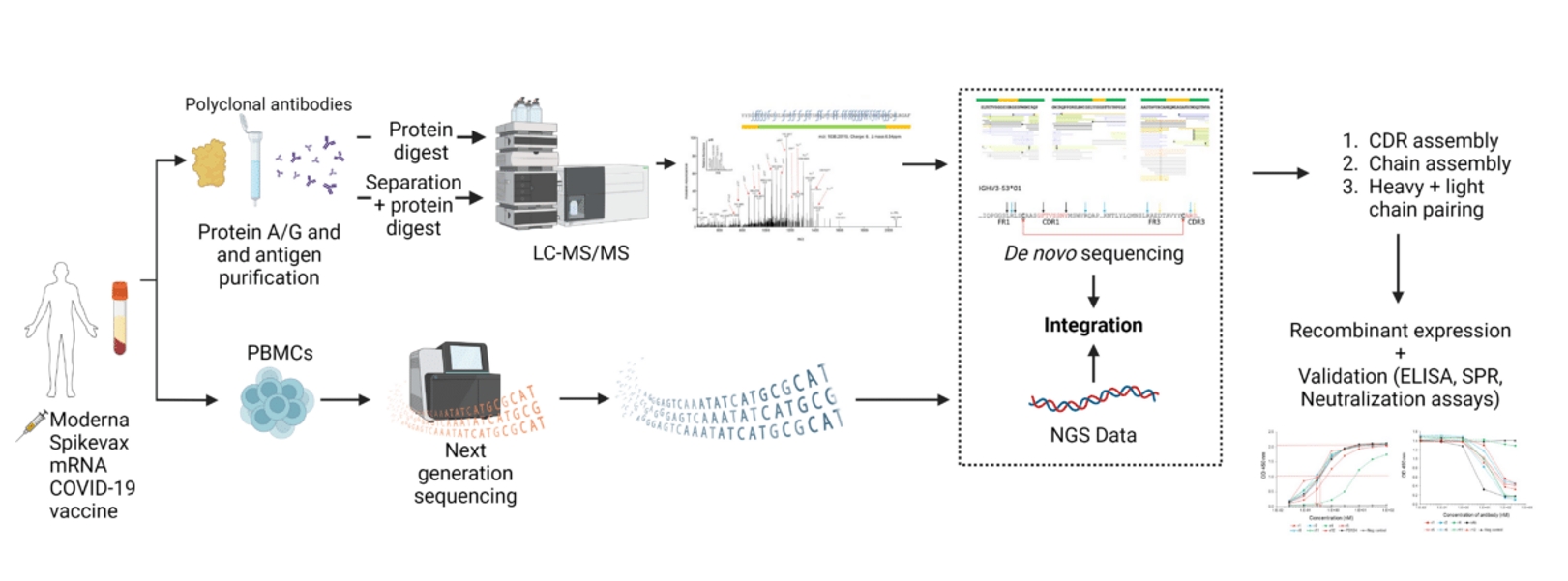
图2 REpAb抗体发现技术可以对人血清多抗测序获得优质中和抗体[2]
参考文献
[1]Townsend DR, Towers DM, Lavinder JJ, Ippolito GC. Innovations and trends in antibody repertoire analysis. Curr Opin Biotechnol. 2024 Apr;86:103082. doi: 10.1016/j.copbio.2024.103082.
[2] Le Bihan T, Nunez de Villavicencio Diaz T, Reitzel C, Lange V, Park M, Beadle E, Wu L, Jovic M, Dubois RM, Couzens AL, Duan J, Han X, Liu Q, Ma B. De novo protein sequencing of antibodies for identification of neutralizing antibodies in human plasma post SARS-CoV-2 vaccination. Nat Commun. 2024 Oct 10;15(1):8790. doi: 10.1038/s41467-024-53105-8.